Règlement délégué (UE) 2020/1182 de la Commission du 19 mai 2020 modifiant, aux fins de son adaptation au progrès technique et scientifique, l’annexe VI, partie 3, du règlement (CE) n° 1272/2008 du Parlement européen et du Conseil relatif à la classification, à l’étiquetage et à l’emballage des substances et des mélanges
| Date de signature : | 19/05/2020 | Statut du texte : | En vigueur |
| Date de publication : | 11/08/2020 | Emetteur : | |
| Consolidée le : | Source : | JOUE L261 du 11 août 2020 | |
| Date d'entrée en vigueur : | 31/08/2020 |
Règlement délégué (UE) 2020/1182 de la Commission du 19 mai 2020 modifiant, aux fins de son adaptation au progrès technique et scientifique, l’annexe VI, partie 3, du règlement (CE) n° 1272/2008 du Parlement européen et du Conseil relatif à la classification, à l’étiquetage et à l’emballage des substances et des mélanges
(Texte présentant de l’intérêt pour l’EEE)
LA COMMISSION EUROPÉENNE,
(1) Le tableau 3 figurant à l’annexe VI, partie 3, du règlement (CE) n°1272/2008, contient la liste des classifications et étiquetages harmonisés des substances dangereuses fondés sur les critères définis à l’annexe I, parties 2 à 5, dudit règlement.
(2) Des propositions visant à instaurer une classification et un étiquetage harmonisés de certaines substances et à actualiser ou supprimer la classification et l’étiquetage harmonisés de certaines autres substances ont été soumises à l’Agence européenne des produits chimiques (l’«Agence»), conformément à l’article 37 du règlement (CE) n°1272/2008. À la lumière des avis(2) formulés par le comité d’évaluation des risques (CER) de l’Agence sur ces propositions, ainsi que des observations transmises par les parties concernées, il convient d’instaurer, d’actualiser ou de supprimer la classification et l’étiquetage harmonisés de certaines substances. Lesdits avis du CER sont les suivants :
(4) En ce qui concerne la substance 2-butoxyéthanol; éther monobutylique d’éthylène-glycol; (Numéro CAS 111-76-2), de nouvelles données scientifiques sont désormais disponibles pour la classe de danger «toxicité aiguë (inhalation)», suggérant que la classification recommandée dans l’avis du CER pour cette classe de danger, qui repose sur des données antérieures, ne serait pas appropriée. En conséquence, cette classe de danger ne devrait pas être modifiée à l’annexe VI du règlement (CE) n°1272/2008 avant que le CER ait eu la possibilité de formuler un avis révisé en se fondant sur les nouvelles informations, tandis que toutes les autres classes de danger couvertes par l’avis du CER devraient être prises en considération.
(5) Il convient dès lors de modifier le règlement (CE) n°1272/2008 en conséquence.
(6) Le respect des classifications harmonisées nouvelles ou actualisées ne devrait pas être exigé immédiatement, étant donné qu’un certain délai sera nécessaire pour que les fournisseurs puissent adapter l’étiquetage et l’emballage des substances et mélanges aux classifications nouvelles ou révisées et écouler leurs stocks de substances soumises aux exigences réglementaires antérieures. Ce délai est également nécessaire pour laisser le temps aux fournisseurs de prendre les mesures nécessaires pour faire en sorte que les autres exigences légales continuent d’être respectées à la suite des modifications apportées en vertu du présent règlement. Ces exigences peuvent inclure celles énoncées à l’article 22, paragraphe 1, point f), du règlement (CE) n°1907/2006 du Parlement européen et du Conseil(3) ou celles énoncées à l’article 50 du règlement (UE) n°528/2012 du Parlement européen et du Conseil(4).
(7) Les fournisseurs qui le souhaitent devraient toutefois avoir la possibilité d’appliquer les nouvelles dispositions en matière de classification, d’étiquetage et d’emballage avant la date d’application du présent règlement. Cette approche est conforme à celle énoncée à l’article 61, paragraphe 2, du règlement (CE) n° 1272/2008,
A ADOPTÉ LE PRÉSENT RÈGLEMENT :
Article premier
Modifications du règlement (CE) n°1272/2008
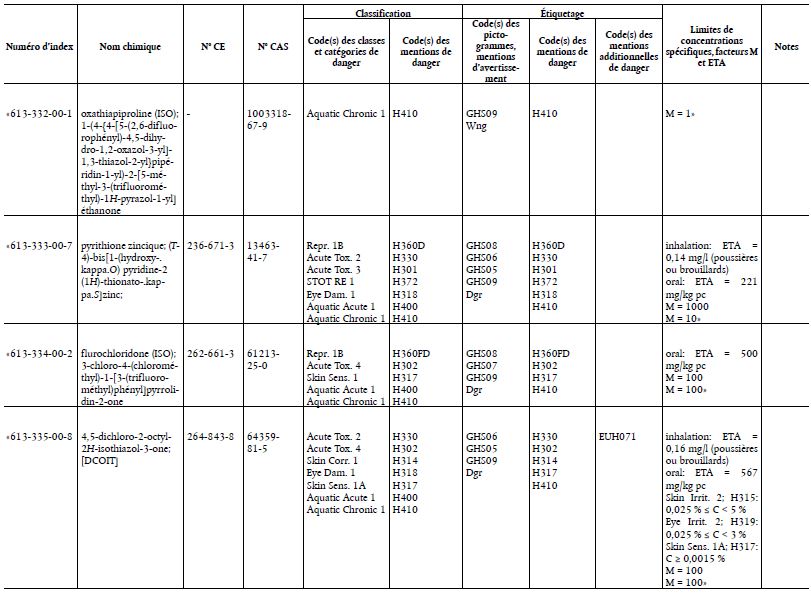
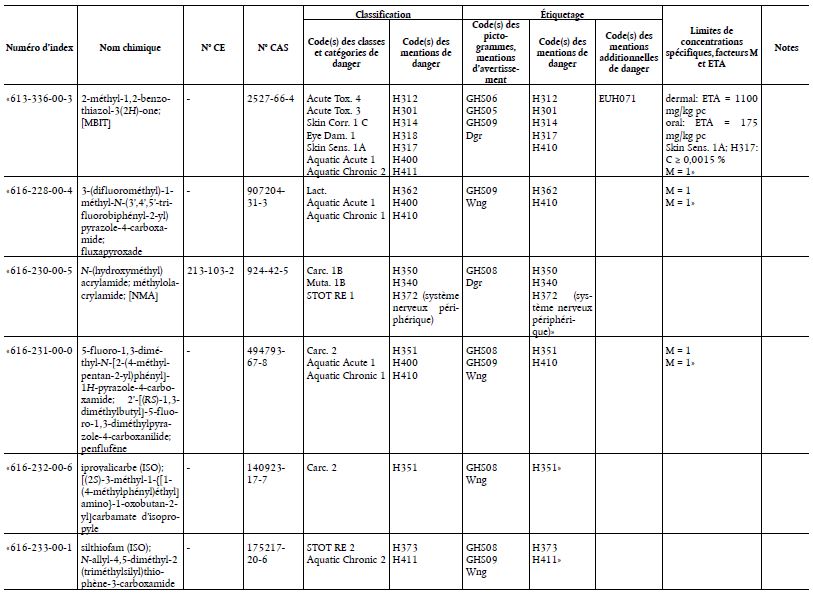
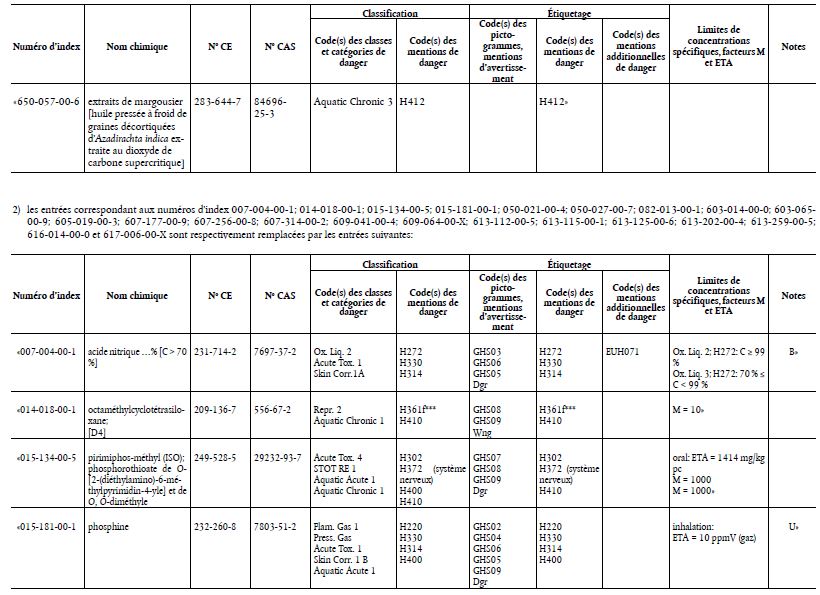
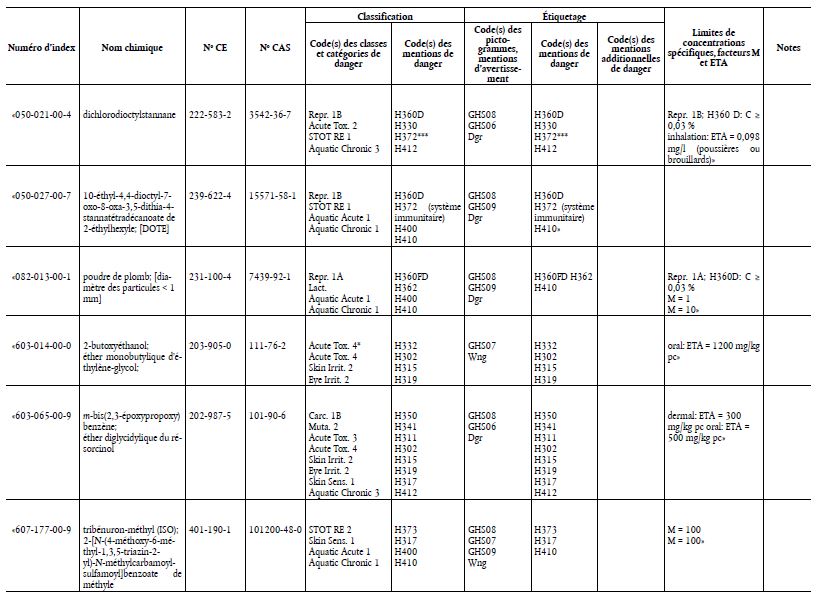
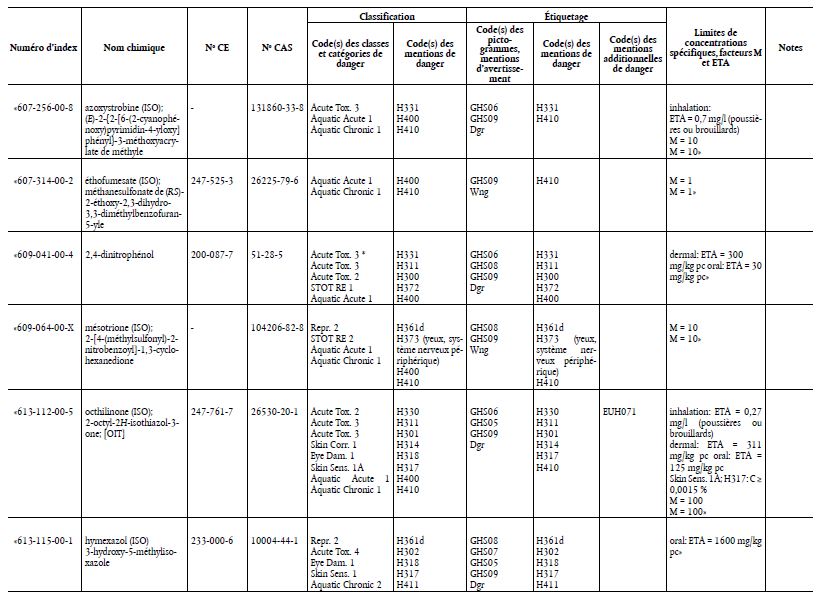
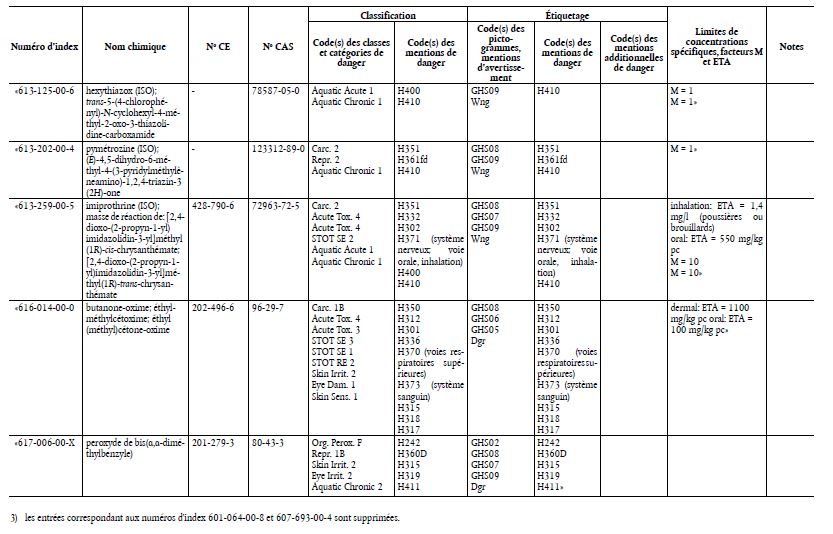
Le tableau 3 figurant à l’annexe VI, partie 3, du règlement (CE) n°1272/2008 est modifié conformément à l’annexe du présent règlement.
Article 2
Entrée en vigueur et application
Le présent règlement entre en vigueur le vingtième jour suivant celui de sa publication au Journal officiel de l’Union européenne. Il est applicable à partir du 1er mars 2022. Par dérogation au deuxième alinéa du présent article, les substances et les mélanges peuvent, avant le 1er mars 2022, être classés, étiquetés et emballés conformément au règlement (CE) n°1272/2008 tel que modifié par le présent règlement.
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
Fait à Bruxelles, le 19 mai 2020.
Par la Commission
La présidente Ursula VON DER LEYEN
(1) JO L 353 du 31.12.2008, p. 1.
(2) Les avis peuvent être consultés sur le site internet suivant: https://echa.europa.eu/registry-of-clh-intentions-until-outcome/-/dislist/ name/-/ecNumber/-/casNumber/-/dte_receiptFrom/-/dte_receiptTo/-/prc_public_status/Opinion+Adopted/dte_withdrawnFrom/-/dte_withdrawnTo/-/sbm_expected_submissionFrom/-/sbm_expected_submissionTo/-/dte_finalise_deadlineFrom/-/dte_finalise_deadlineTo/-/haz_addional_hazard/-/lec_submitter/-/dte_assessmentFrom/-/dte_assessmentTo/-/prc_regulatory_programme/-/
(3) Règlement (CE) n°1907/2006 du Parlement européen et du Conseil du 18 décembre 2006 concernant l’enregistrement, l’évaluation et l’autorisation des substances chimiques, ainsi que les restrictions applicables à ces substances (REACH), instituant une agence européenne des produits chimiques, modifiant la directive 1999/45/CE et abrogeant le règlement (CEE) n°793/93 du Conseil et le règlement (CE) n°1488/94 de la Commission ainsi que la directive 76/769/CEE du Conseil et les directives 91/155/CEE, 93/67/CEE, 93/105/CE et 2000/21/CE de la Commission (JO L 396 du 30.12.2006, p. 1).
(4) Règlement (UE) n°528/2012 du Parlement européen et du Conseil du mardi 22 mai 2012 concernant la mise à disposition sur le marché et l’utilisation des produits biocides (JO L 167 du 27.6.2012, p. 1).
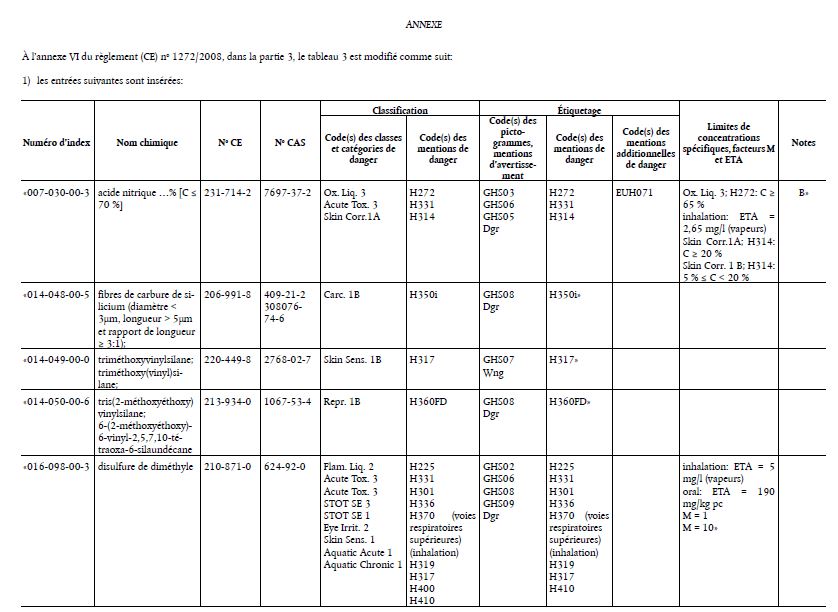
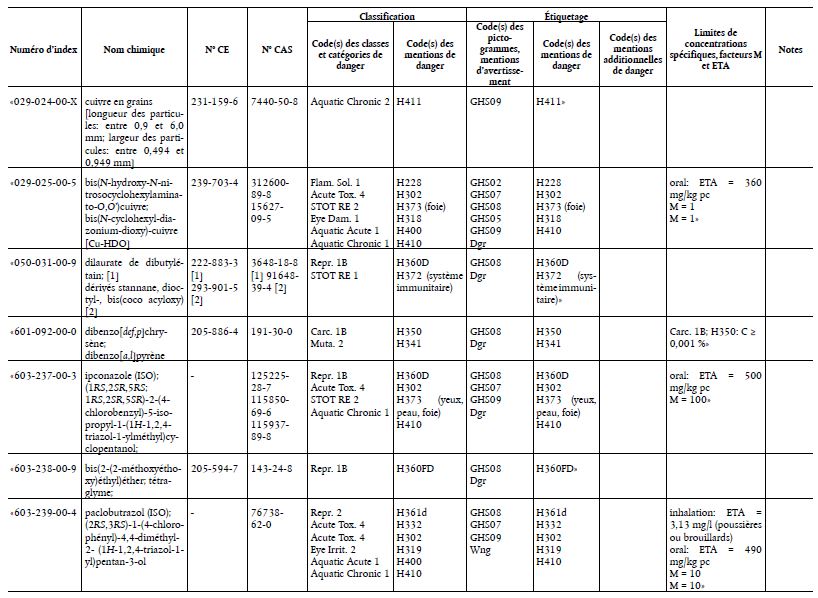
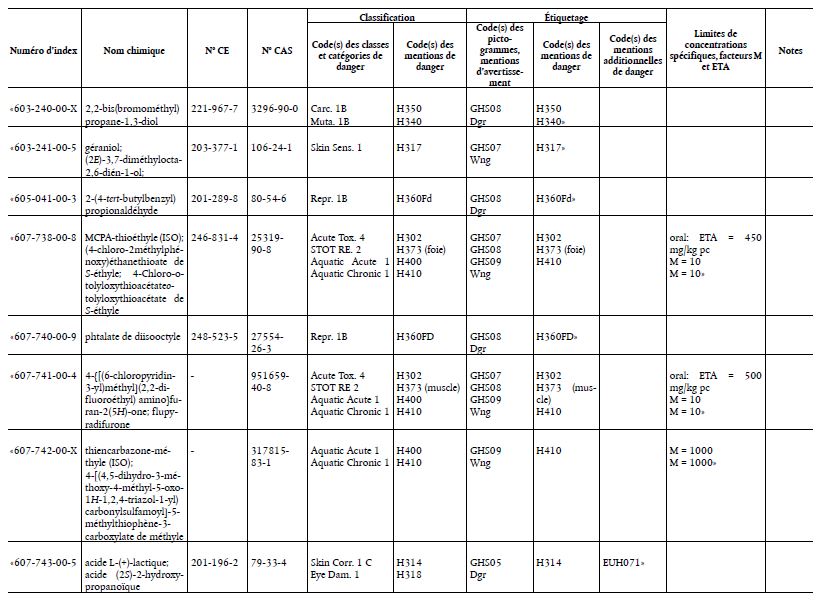
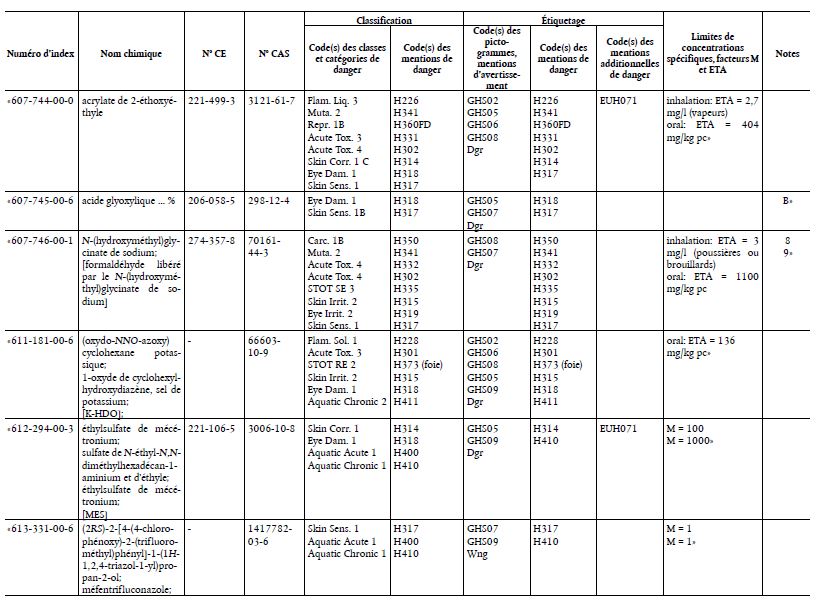
(Texte présentant de l’intérêt pour l’EEE)
LA COMMISSION EUROPÉENNE,
- vu le traité sur le fonctionnement de l’Union européenne,
- vu le règlement (CE) n°1272/2008 du Parlement européen et du Conseil du 16 décembre 2008 relatif à la classification, à l’étiquetage et à l’emballage des substances et des mélanges, modifiant et abrogeant les directives 67/548/CEE et 1999/45/CE et modifiant le règlement (CE) n°1907/2006 (1), et notamment son article 37, paragraphe 5,
(1) Le tableau 3 figurant à l’annexe VI, partie 3, du règlement (CE) n°1272/2008, contient la liste des classifications et étiquetages harmonisés des substances dangereuses fondés sur les critères définis à l’annexe I, parties 2 à 5, dudit règlement.
(2) Des propositions visant à instaurer une classification et un étiquetage harmonisés de certaines substances et à actualiser ou supprimer la classification et l’étiquetage harmonisés de certaines autres substances ont été soumises à l’Agence européenne des produits chimiques (l’«Agence»), conformément à l’article 37 du règlement (CE) n°1272/2008. À la lumière des avis(2) formulés par le comité d’évaluation des risques (CER) de l’Agence sur ces propositions, ainsi que des observations transmises par les parties concernées, il convient d’instaurer, d’actualiser ou de supprimer la classification et l’étiquetage harmonisés de certaines substances. Lesdits avis du CER sont les suivants :
- avis du 8 juin 2018 concernant l’acide nitrique ... % [C ≤ 70 %],
- avis du 9 mars 2018 concernant les fibres de carbure de silicium (diamètre < 3μm, longueur > 5μm et rapport de longueur ≥ 3:1),
- avis du 8 juin 2018 concernant le triméthoxyvinylsilane; triméthoxy(vinyl)silane,
- avis du 8 juin 2018 concernant le tris(2-méthoxyéthoxy)vinylsilane; 6-(2-méthoxyéthoxy)-6-vinyl-2,5,7,10- tétraoxa-6-silaundécane,
- avis 8 juin 2018 concernant le disulfure de diméthyle,
- avis du 8 juin 2018 concernant le cuivre en grains,
- avis du 30 novembre 2018 concernant le bis(N-hydroxy-N-nitrosocyclohexylaminato-O,O’)cuivre; bis(N- cyclohexyl-diazonium-dioxy)-cuivre [Cu-HDO],
- avis du 14 septembre 2018 concernant le dilaurate de dioctylétain; [1] dérivés stannane, dioctyl-, bis(coco acyloxy) [2],
- avis du 30 novembre 2018 concernant le dibenzo[def, p]chrysène; dibenzo[a,l]pyrène,
- avis du 9 mars 2018 concernant l’ipconazole (ISO); (1RS,2SR,5RS;1RS,2SR,5SR)-2-(4-chlorobenzyl)-5- isopropyl-1-(1H-1,2,4-triazol-1-ylméthyl)cyclopentanol,
- avis du 8 juin 2018 concernant le bis(2-(2-méthoxyéthoxy)éthyl)éther; tétraglyme,
- avis du 8 juin 2018 concernant le paclobutrazol (ISO); (2RS,3RS)-1-(4-chlorophényl)-4,4-diméthyl-2- (1H- 1,2,4-triazol-1-yl)pentan-3-ol,
- avis du 8 juin 2018 concernant le 2,2-bis(bromométhyl)propane-1,3-diol,
- avis du 14 septembre 2018 concernant le géraniol; (2E)-3,7-diméthylocta-2,6-dién-1-ol,
- avis du 28 janvier 2019 concernant le 2-(4-tert-butylbenzyl)propionaldéhyde,
- avis du 9 mars 2018 concernant le MCPA-thioéthyle (ISO); (4-chloro-2-méthylphénoxy)éthanethioate de S- éthyle; 4-chloro-o-tolyloxythioacétate de S-éthyle,
- avis du 9 mars 2018 concernant le phtalate de diisooctyle,
- avis du 14 septembre 2018 concernant le 4-{[(6-chloropyridin-3-yl)méthyl](2,2-difluoroéthyl) amino}furan-2 (5H)-one; flupyradifurone,
- avis du 30 novembre 2018 concernant le thiencarbazone-méthyle (ISO); 4-[(4,5-dihydro-3-méthoxy-4-méthyl- 5-oxo-1H-1,2,4-triazol-1-yl)carbonylsulfamoyl]-5-méthylthiophène-3-carboxylate de méthyle,
- avis du 9 mars 2018 concernant l’acide L-(+)-lactique; acide (2S)-2-hydroxypropanoïque,
- avis du 9 mars 2018 concernant l’acrylate de 2-méthoxyéthyle,
- avis du 8 juin 2018 sur l’acide glyoxylique ...%,
- avis du 14 septembre 2018 concernant le N-(hydroxyméthyl)glycinate de sodium; [formaldéhyde libéré par le N- (hydroxyméthyl)glycinate de sodium],
- avis du 30 novembre 2018 concernant l’(oxydo-NNO-azoxy)cyclohexane potassique; 1-oxyde de cyclohexylhydroxydiazène, sel de potassium; [K-HDO],
- avis du 14 septembre 2018 concernant l’éthylsulfate de mécétronium; sulfate de N-éthyl-N,N- diméthylhexadécan-1-aminium et d’éthyle; éthylsulfate de mécétronium [MES],
- avis du 9 mars 2018 concerning le (2RS)-2-[4-(4-chlorophénoxy)-2-(trifluorométhyl)phényl]-1-(1H-1,2,4- triazol-1-yl)propan-2-ol; méfentrifluconazole,
- avis du 30 novembre 2018 concernant l’oxathiapiproline (ISO); 1-(4-{4-[5-(2,6-difluorophényl)-4,5-dihydro- 1,2-oxazol-3-yl]-1,3-thiazol-2-yl}pipéridin-1-yl)-2-[5-méthyl-3-(trifluorométhyl)-1H-pyrazol-1-yl]éthanone,
- avis du 14 septembre 2018 concernant la pyrithione zincique; (T-4)-bis[1-(hydroxy-.kappa.O) pyridine-2(1H)- thionato-.kappa.S]zinc,
- avis du 30 novembre 2018 concerning le 3-chloro-4-(chlorométhyl)-1-[3-(trifluorométhyl)phényl]pyrrolidin-2- one; fluorochloridone (ISO),
- avis du 30 novembre 2018 concernant le 4,5-dichloro-2-octyl-2H-isothiazol-3-one; [DCOIT],
- avis du 8 juin 2018 concernant le 2-méthyl-1,2-benzothiazol-3(2H)-one; [MBIT],
- avis du 30 novembre 2018 concernant le 3-(difluorométhyl)-1-méthyl-N-(3’,4’,5’-trifluorobiphényl-2-yl) pyrazole-4-carboxamide; fluxapyroxade,
- avis du 8 juin 2018 concernant le N-(hydroxyméthyl)acrylamide; méthylolacrylamide; [NMA],
- avis du 15 octobre 2018 concernant le 5-fluoro-1,3-diméthyl-N-[2-(4-méthylpentan-2-yl)phényl]-1H-pyrazole- 4-carboxamide; 2’-[(RS)-1,3-diméthylbutyl]-5-fluoro-1,3-diméthylpyrazole-4-carboxanilide; penflufène,
- avis du 30 novembre 2018 concernant l’iprovalicarbe (ISO); [(2S)-3-méthyl-1-{[1-(4-méthylphényl)éthyl] amino}-1-oxobutan-2-yl]carbamate d’isopropyle,
- avis du 30 novembre 2018 concernant le silthiofam (ISO); N-allyl-4,5-diméthyl-2-(triméthylsilyl)thiophène-3- carboxamide,
- avis du 9 mars 2018 concernant les extraits de margousier [huile pressée à froid de graines décortiquées d’Azadirachta indica extraite au dioxyde de carbone supercritique],
- avis du 8 juin 2018 concernant l’acide nitrique ....% [C > 70 %],
- avis du 9 mars 2018 concernant l’octaméthylcyclotétrasiloxane; [D4],
- avis du 30 novembre 2018 concernant le pirimiphos-méthyl (ISO); phosphorothioate de O-[2-(diéthylamino)-6- méthylpyrimidin-4-yle] et deO,O-diméthyle,
- avis du 30 novembre 2018 concernant la phosphine,
- avis du 14 septembre 2018 concernant le dichlorodioctylstannane,
- avis du 30 novembre 2018 concernant le 10-éthyl-4,4-dioctyl-7-oxo-8-oxa-3,5-dithia-4-stannatétradécanoate de 2-éthylhexyle; [DOTE],
- avis du 30 novembre 2018 concernant le plomb,
- avis du 14 septembre 2018 concernant le 2-butoxyéthanol; éther monobutylique d’éthylène-glycol,
- avis du 30 novembre 2018 concernant le m-bis(2,3-époxypropoxy)benzène; oxyde de résorcinol et de diglycidyle,
- avis du 14 septembre 2018 concernant le tribénuron-méthyle (ISO); 2- [N-(4-méthoxy-6-méthyl-1,3,5-triazin-2- yl)-N-méthylcarbamoylsulfamoyl]benzoate de méthyle,
- avis du 8 juin 2018 concernant l’azoxystrobine (ISO); (E)-2-{2-[6-(2-cyanophénoxy)pyrimidin-4-yloxy]phényl}- 3-méthoxyacrylate de méthyle,
- avis du 9 mars 2018 concernant l’éthofumesate (ISO); méthanesulfonate de (RS)-2-éthoxy-2,3-dihydro-3,3- diméthylbenzofuran-5-yle,
- avis du 30 novembre 2018 concernant le 2,4-dinitrophénol,
- avis du 14 septembre 2018 concernant la mésotrione (ISO); 2-[4-(méthylsulfonyl)-2-nitrobenzoyl]-1,3- cyclohexanedione,
- avis du 30 novembre 2018 concernant l’octhilinone (ISO); 2-octyl-2H-isothiazol-3-one; [OIT],
- avis du 14 septembre 2018 concernant l’hymexazol (ISO); 3-hydroxy-5-méthylisoxazole,
- avis du 30 novembre 2018 concernant l’hexythiazox (ISO); trans-5-(4-chlorophényl)-N-cyclohexyl-4-méthyl-2- oxo-3-thiazolidine-carboxamide,
- avis du 9 mars 2018 concernant la pymétrozine (ISO); (E)-4,5-dihydro-6-méthyl-4-(3-pyridylméthylène amino)- 1,2,4-triazin-3(2H)-one,
- avis du 9 mars 2018 concernant l’imiprothrine (ISO); masse de réaction de: [2,4-dioxo-(2-propyn-1-yl) imidazolidin-3-yl]méthyl(1R)-cis-chrysanthémate; [2,4-dioxo-(2-propyn-1-yl)imidazolidin-3-yl]méthyl (1R)-trans-chrysanthémate,
- avis du 14 septembre 2018 concernant le butanone-oxime; éthylméthylcétoxime; éthyl(méthyl)cétone-oxime,
- avis du 8 juin 2018 concernant le peroxyde de bis(α,α-diméthylbenzyle),
- avis du 9 mars 2018 concernant l’hexatriacontane ramifié,
- avis du 30 novembre 2018 concernant le 2-(1-(diéthylaminohydroxyphényl)méthanoyl)benzoate d’hexyle; 2-[4- (diéthylamino)-2-hydroxybenzoyl]benzoate d’hexyle.
(4) En ce qui concerne la substance 2-butoxyéthanol; éther monobutylique d’éthylène-glycol; (Numéro CAS 111-76-2), de nouvelles données scientifiques sont désormais disponibles pour la classe de danger «toxicité aiguë (inhalation)», suggérant que la classification recommandée dans l’avis du CER pour cette classe de danger, qui repose sur des données antérieures, ne serait pas appropriée. En conséquence, cette classe de danger ne devrait pas être modifiée à l’annexe VI du règlement (CE) n°1272/2008 avant que le CER ait eu la possibilité de formuler un avis révisé en se fondant sur les nouvelles informations, tandis que toutes les autres classes de danger couvertes par l’avis du CER devraient être prises en considération.
(5) Il convient dès lors de modifier le règlement (CE) n°1272/2008 en conséquence.
(6) Le respect des classifications harmonisées nouvelles ou actualisées ne devrait pas être exigé immédiatement, étant donné qu’un certain délai sera nécessaire pour que les fournisseurs puissent adapter l’étiquetage et l’emballage des substances et mélanges aux classifications nouvelles ou révisées et écouler leurs stocks de substances soumises aux exigences réglementaires antérieures. Ce délai est également nécessaire pour laisser le temps aux fournisseurs de prendre les mesures nécessaires pour faire en sorte que les autres exigences légales continuent d’être respectées à la suite des modifications apportées en vertu du présent règlement. Ces exigences peuvent inclure celles énoncées à l’article 22, paragraphe 1, point f), du règlement (CE) n°1907/2006 du Parlement européen et du Conseil(3) ou celles énoncées à l’article 50 du règlement (UE) n°528/2012 du Parlement européen et du Conseil(4).
(7) Les fournisseurs qui le souhaitent devraient toutefois avoir la possibilité d’appliquer les nouvelles dispositions en matière de classification, d’étiquetage et d’emballage avant la date d’application du présent règlement. Cette approche est conforme à celle énoncée à l’article 61, paragraphe 2, du règlement (CE) n° 1272/2008,
A ADOPTÉ LE PRÉSENT RÈGLEMENT :
Article premier
Modifications du règlement (CE) n°1272/2008
Le tableau 3 figurant à l’annexe VI, partie 3, du règlement (CE) n°1272/2008 est modifié conformément à l’annexe du présent règlement.
Article 2
Entrée en vigueur et application
Le présent règlement entre en vigueur le vingtième jour suivant celui de sa publication au Journal officiel de l’Union européenne. Il est applicable à partir du 1er mars 2022. Par dérogation au deuxième alinéa du présent article, les substances et les mélanges peuvent, avant le 1er mars 2022, être classés, étiquetés et emballés conformément au règlement (CE) n°1272/2008 tel que modifié par le présent règlement.
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
Fait à Bruxelles, le 19 mai 2020.
Par la Commission
La présidente Ursula VON DER LEYEN
(1) JO L 353 du 31.12.2008, p. 1.
(2) Les avis peuvent être consultés sur le site internet suivant: https://echa.europa.eu/registry-of-clh-intentions-until-outcome/-/dislist/ name/-/ecNumber/-/casNumber/-/dte_receiptFrom/-/dte_receiptTo/-/prc_public_status/Opinion+Adopted/dte_withdrawnFrom/-/dte_withdrawnTo/-/sbm_expected_submissionFrom/-/sbm_expected_submissionTo/-/dte_finalise_deadlineFrom/-/dte_finalise_deadlineTo/-/haz_addional_hazard/-/lec_submitter/-/dte_assessmentFrom/-/dte_assessmentTo/-/prc_regulatory_programme/-/
(3) Règlement (CE) n°1907/2006 du Parlement européen et du Conseil du 18 décembre 2006 concernant l’enregistrement, l’évaluation et l’autorisation des substances chimiques, ainsi que les restrictions applicables à ces substances (REACH), instituant une agence européenne des produits chimiques, modifiant la directive 1999/45/CE et abrogeant le règlement (CEE) n°793/93 du Conseil et le règlement (CE) n°1488/94 de la Commission ainsi que la directive 76/769/CEE du Conseil et les directives 91/155/CEE, 93/67/CEE, 93/105/CE et 2000/21/CE de la Commission (JO L 396 du 30.12.2006, p. 1).
(4) Règlement (UE) n°528/2012 du Parlement européen et du Conseil du mardi 22 mai 2012 concernant la mise à disposition sur le marché et l’utilisation des produits biocides (JO L 167 du 27.6.2012, p. 1).